Alexis St-Gelais, chimiste – Vulgarisation & Capsule végétale
La sélection intensive à laquelle est soumise le cannabis produit des variétés (strains) présentant des signatures moléculaires variées, et c’est particulièrement apparent lorsque l’on s’attarde aux profils des terpènes. Ces spécificités peuvent être utiles pour caractériser une lignée ou un extrait, en mettant de l’avant ce qui le rend unique par rapport à une autre variété. Sur la base de notre vaste expérience avec les terpènes du cannabis, voyons ensemble quelques tendances moléculaires intéressantes dans cette plante.
Chémotypes et cannabis
La production de molécules dans une plante obéit à une logique métabolique. Un parallèle grossier peut être fait avec la couleur des yeux des humains: en fonction des caractéristiques génétiques d’un individu, notre corps dispose ou non de la capacité de générer des pigments qui détermineront à leur tour la teinte de l’iris. Celle-ci (bien qu’avec bien des nuances) peut être classifiée dans un nombre limité de catégories, comme yeux bleus. Pour étudier les plantes, le concept de chémotype peut être utilisé pour désigner ce phénomène où des molécules sont présentes chez certains individus et pas (ou peu) chez d’autres. Polatoglu a suggéré la définition suivante pour ce concept (traduction libre): organismes catégorisés comme faisant partie de la même espèce […] et présentant des différences en quantité et qualité de leur(s) composant(s) dans leur empreinte chimique totale, ces différences étant liées à la génétique ou à des différences d’expression génétique [1].
Chez le cannabis, l’expression des cannabinoïdes tend à suivre des patrons chémotypiques, où un ou deux cannabinoïdes dominants sont observés et peuvent varier d’une lignée à l’autre. Dans The Handbook of Cannabis, de Meijer propose un modèle comprenant trois facteurs génétiques et un facteur morphologique qui peuvent conduire une variété donnée à exprimer une de neuf possibilités de chémotypes (ou encore davantage, puisqu’on peut observer des chémotypes mixtes où deux molécules sont codominantes, le plus typiquement le THCA et le CBDA) [2]. Ce modèle est résumé à la figure 1 ci-dessous, où le terme « locus » réfère à une zone d’un chromosome du plant de cannabis où les gènes présents influenceront l’expression métabolique des cannabinoïdes.

Figure 1. Modèle génétique proposé par de Meijer [2] (figure adaptée par PhytoChemia) pour expliquer les chémotypes de cannabinoïdes. Un premier locus contrôle l’expression d’enzymes qui sont nécessaires à la synthèse des précurseurs métaboliques de la portion phénolique des cannabinoïdes – ci ce locus est inactif, la plante n’aura pas accès aux matières premières métaboliques requises et aucun cannabinoïde ne sera produit. Un second locus contrôle la longueur de la chaîne carbonée attachée à ce squelette phénolique, définissant une proportion entre les acides phénoliques C3 et C5 (respectivement acides divarinolique et olivétolique, ce dernier constituant le précurseur des THCA et CBDA usuels). Un troisième locus fonctionne selon un schéma semblable à celui des groupes sanguins A/B/AB/O chez l’humain (ce parallèle est de nous, et non de de Meijer). Si le locus est inactif (à l’image du type sanguin O), le métabolisme s’arrête au CBGA (ou au CBGVA); lorsque l’information génétique du type A est présente, du THCA est produit, alors que le type B permet la synthèse de CBDA (et les deux types peuvent être présents, comme pour le groupe sanguin AB, produisant un chémotype mixte). Un quatrième paramètre peut entrer en jeu et a trait à la morphologie des trichromes, qui peut dans certains cas entraîner la conversion du CBGA en CBCA et produire davantage de chémotypes.
Pour autant que nous sachions, un tel modèle intégré pour les terpènes du cannabis reste à être défini (laissez-nous savoir si vous en connaissez un!). Vous pouvez néanmoins constater à partir de l’exemple des cannabinoïdes que les traits génétiques d’une variété peuvent définir si, oui ou non, une molécule s’accumulera comme résultante du métabolisme d’une plante – ou, en d’autres termes, si une variété appartiendra à un chémotype donné.
Terpènes corrélés
Bien souvent, une transformation métabolique donnée est effectuée grâce à une enzyme, c’est-à-dire une protéine qui est capable de faciliter une transformation chimique particulière. Les enzymes peuvent être plus ou moins sélectives quant aux molécules qu’elles peuvent transformer. Lorsque plusieurs molécules présentent une structure similaire, elles peuvent parfois toutes être transformées par une même enzyme, bien que pas forcément toutes à la même vitesse ou avec la même efficacité. Cela implique que si une plante exprime une enzyme particulière grâce à ses traits génétiques, il arrive que parfois non pas une mais plusieurs molécules puissent en résulter. Dans d’autres cas, si une enzyme permet la transformation d’une molécule clé en amont, plusieurs transformations en aval peuvent devenir possibles puisque la « matière première » devient disponible. Dans tous les cas, même sans connaître le détail des mécanismes métaboliques et génétiques en jeu, on peut observer s’il existe des corrélations entre des molécules, ce qui impliquerait qu’elles ont une origine commune. Si cela s’avère, on devrait considérer ces composés ensemble, puisqu’il est peu probable d’un observer un et non les autres.
Il existe plusieurs exemples de ce tels groupes parmi les terpènes du cannabis. Voici certains groupes quantitativement importants à garder à l’oeil:
- • Les pinènes sont corrélés entre eux, avec des proportions variables des isomères α- et β-;
- • Lorsque le limonène est abondant, une série de monoterpènes oxygénés tend à également présenter une teneur plus élevée;
- • Une forte proportion de terpinolène sera accompagnée par la présence de plusieurs autres monoterpènes;
- • Le β-caryophyllène et l’α-humulène sont fortement corrélés;
- • Un groupe de sesquiterpènes de type eudésmane (ou sélinane) sont étroitement liés. Il comprend les α- and β-sélinènes, quelques isomères de sélinadiènes et le camphre genévrier (juniper camphor). Ils corrèlent également avec le spirovétiva-1(10),7(11)-diène et l’érémophila-1(10),7(11)-diène;
- • Les α- et δ-guaiènes sont observés ensemble;
- • Le germacrène B est toujours associé au γ-élémène lors des analyses par GC, puisque ce dernier est un produit de dégradation thermique du germacrène B et ainsi systématiquement généré pendant l’analyse. Le (E)-α-bisabolène et l’α-bisabolol tendent à partiellement corréler avec le germacrène B;
- • Enfin, une grappe de sesquiterpénols comprenant le guaiol, les eudésmols, le bulnésol et le cryptoméridiol sont clairement liés lest uns aux autres en matière d’abondance.
Comportement des groupes de terpènes d’une variété à l’autre
Au fil de nos analyses sur des milliers d’échantillons, certaines tendances sont devenus apparentes au sein des groupes décrits plus haut. Voici certains phénomènes que nous observons au fil de nos analyses. Gardez en tête qu’avec la sélection intensive, un producteur peut toujours tomber sur quelque chose d’inhabituel: les éléments ci-dessous sont des tendances, pas des règles absolues!
Monoterpènes
Le profil des terpènes est la plupart du temps dominé par un ou plusieurs des monoterpènes suivants: myrcène, α-pinène*, limonène*, terpinolène*, (E)-β-ocimène et linalol – ces deux derniers étant très rarement le composé dominant. Souvenez-vous que les molécules marquées d’une astérisque sont accompagnées au sein de leur groupe. Sous l’angle des tendances métaboliques, les cas du terpinolène et du limonène sont particulièrement intéressants.
Du côté du terpinolène, sa présence semble être une clé métabolique pour l’expression de nombreuses autres molécules. Dès lors que le terpinolène est un terpène dominant, un groupe diversifié de terpènes qui ne sont habituellement rencontrés qu’à l’état de traces se font plus visibles. Certains d’entre eux sont représentés à la figure 2.

Figure 2. Composés associés au terpinolène dans le cannabis. Ces molécules tendent à être plus abondantes dès lors qu’une variété est riche en terpinolène, et sont autrement trouvés à l’état de traces voir carrément absents. En plus de ces molécules, un monoterpène oxygéné inconnu est également étroitement lié au terpinolène. Il est élué près du terpinén-4-ol sur une colonne de type DB-5.
Quant au limonène, sa concentration est corrélée avec celle du camphène et de plusieurs monoterpènes oxygénés, incluant l’α-terpinéol, l’endo-fenchol et le bornéol, ainsi que les hydrates de pinène (figure 3). Ces derniers sont peu courants dans le domaine des huiles essentielles, le cannabis étant l’une des rares sources botaniques où ils sont présents avec une certaine abondance aux côté de l’inhabituelle sauge sauvage africaine (ou leleshwa) Tarchonanthus camphoratus.

Figure 3. Structures des molécules corrélées à l’abondance du limonène dans le cannabis.
Sesquiterpènes
β-Caryophyllène and α-Humulène
Ces deux sesquiterpènes (figure 4) peuvent parfois surpasser les monoterpènes en ce qui a trait à la concentration dans une variété. Ils sont toujours exprimés, à moins qu’une variété ou un extrait ne soit presque totalement dépourvu de terpènes. Cela n’est pas surprenant, puisque ces terpènes figurent parmi les plus largement distribués dans la nature – somme toute, assez peu de plantes produisant des huiles essentielles ne les expriment pas. Il est particulièrement rare de croiser du cannabis où la somme de caryophyllène et d’humulène ne représente pas au moins 1% (en pourcentage relatif) des terpènes totaux, et ils peuvent se retrouver à peu près partout le long de leur gradient possible de concentrations. Ainsi, ils ne font pas vraiment partie d’un chémotype, mais plutôt d’un continuum.
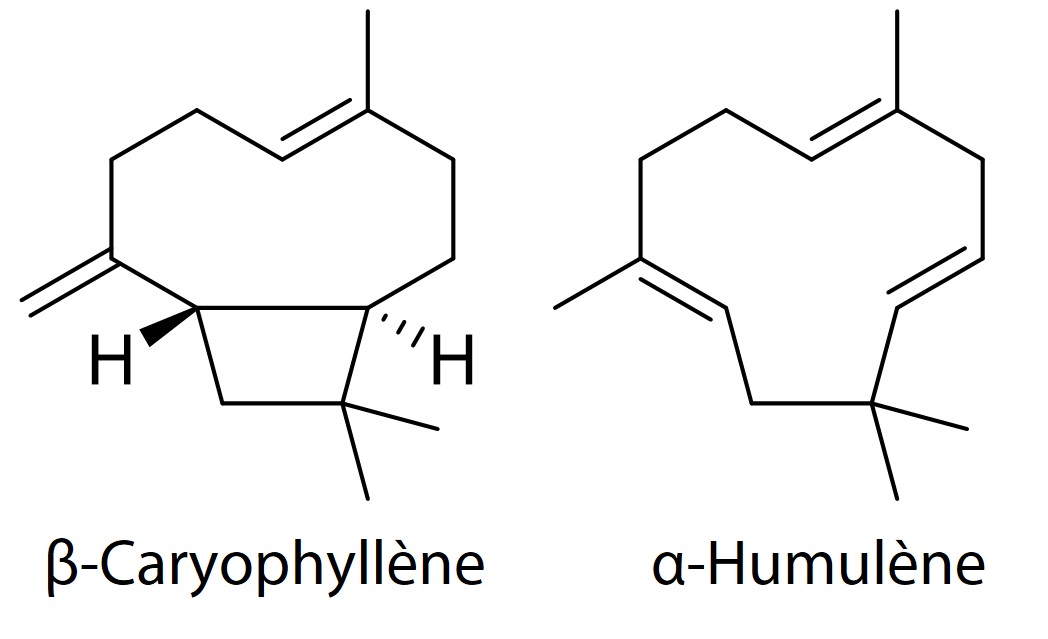
Figure 4. Structures du β-caryophyllène et de l’α-humulène
Germacrène B
Comme mentionné plus haut, le germacrène B n’est pas thermiquement stable (figure 5). Dès qu’on l’observe sur un profil d’analyse par GC, il sera inévitablement accompagné par le γ-élémène, produit par dégradation partiellement du germacrène B au sein du port d’injection chauffé de l’instrument [3]. Ces terpènes ne font habituellement pas partie des cibles criblées par la plupart des laboratoires, puisque le standard de germacrène B est difficile à obtenir – mais il peut néanmoins être une composante quantitativement importante parmi les terpènes pour certains variétés. Nous avons vu la somme des germacrène B et γ-élémène dépasser sensiblement les 10 mg/g dans certains cas! Il y a également des variétés où on retrouve à peine le germacrène B, ainsi que presque toutes les possibilités entre ces deux extrêmes.
Il existe un certain degré de corrélation entre le germacrène B et une paire de composés étroitement liés, le (E)-α-bisabolène et l’α-bisabolol, bien que dans certains cas nous observions des exemples où ils sont découplés. Le duo α-bisabolène/α-bisabolol présente un comportement chémotypique, alors qu’ils sont exprimés dans la plupart des variétés, mais de temps à autre inhibés vers de très faibles teneurs.

Figure 5. Structures du germacrène B et de composés fortement ou partiellement corrélés avec celui-ci.
Guaiènes
L’α-guaiène et le δ-guaiène (figure 6) sont typiquement rencontrés dans les huiles essentielles de rose et de patchouli, notamment. Chez plusieurs variétés de cannabis, ces sesquiterpènes ne seront que faiblement exprimés, mais dans quelques cas, leur expression se déclenche jusqu’à ce qu’ils représentent quelques points de pourcentage relatif des terpènes totaux. En toute honneteté, il est difficile de suivre l’α-guaiène, puisqu’il tend à coéluer avec un autre sesquiterpène quantitativement abondant du cannabis, le trans-α-bergamotène, sur plusieurs colonnes GC (incluant les phases DB-5 et DB-Wax). Le δ-guaiène est donc le composé à suivre pour constater ce chémotype. Il existe des exceptions, mais les guaiènes vont typiquement se retrouver soit sous les 0.5 mg/g, soit dans une fourchette comprise entre 1 et 3 mg/g, ce qui suggère qu’un trait génétique va soit permettre, soit inhiber leur production. L’α-guaiène peut s’oxyder avec le temps pour générer un composé fortement odorant, la rotundone [4] – cette dernière est probablement trop peu abondante pour être suivie directement dans le cannabis, mais pourrait contribuer à l’arôme de certaines variétés.

Figure 6. Structures des guaiènes.
Eudésmanes (Sélinanes)
Voilà un groupe de sesquiterpènes (figure 7) que vous ne voulez pas manquer si vous chercher à obtenir une teneur représentative de terpènes pour une variété. Les sélinadiènes sont, pour plusieurs d’entre elles, parmi les terpènes les plus abondants de l’ensemble, contribuant parfois à bien au-delà de 10 mg/g au total. Pour autant que nous sachions, le cannabis est d’ailleurs la plante où ces molécules sont les plus abondantes. Le fait que notre service de criblage de terpènes les prenne en compte alors que la plupart des laboratoires les ignorent explique en bonne partie les différences entre les teneurs rapportées de « terpènes totaux » – gardez en tête que le concept de terpènes totaux est à utiliser avec précautions.

Figure 7. Structures des principaux sesquiterpènes de type eudésmane trouvés dans le cannabis, ainsi que des substances corrélées spirovetiva-1(10),7(11)-diène et érémophila-1(10),7(11)-diène. Le groupe comprend également le sélina-4,7(11)-diène.
Il semble y avoir des chémotypes dans le cas des eudésmanes, également. Dans quelques variétés, ils sont quasiment absents, ce qui suggère que l’absence d’un gène particulier inhibe leur métabolisme.
Sesquiterpénols du groupe bulnésol/guaiol/eudésmols
Un dernier groupe digne d’intérêt comprend plusieurs molécules étroitement corrélées (figure 8), incluant le bulnésol, le guaiol, et plusieurs isomères d’eudésmols. À l’exception du cryptoméridiol, on les trouve tous sensiblement dans les mêmes teneurs, et ils suivent un patron chémotypique de type présence/absence. Certaines variétés expriment clairement ce groupe, alors que les molécules ne se trouvent qu’à l’état de traces dans d’autres cas. Suivant notre expérience, c’est l’un des traits métaboliques les plus variables entre les variétés, aux côtés de l’identité du monoterpène dominant.
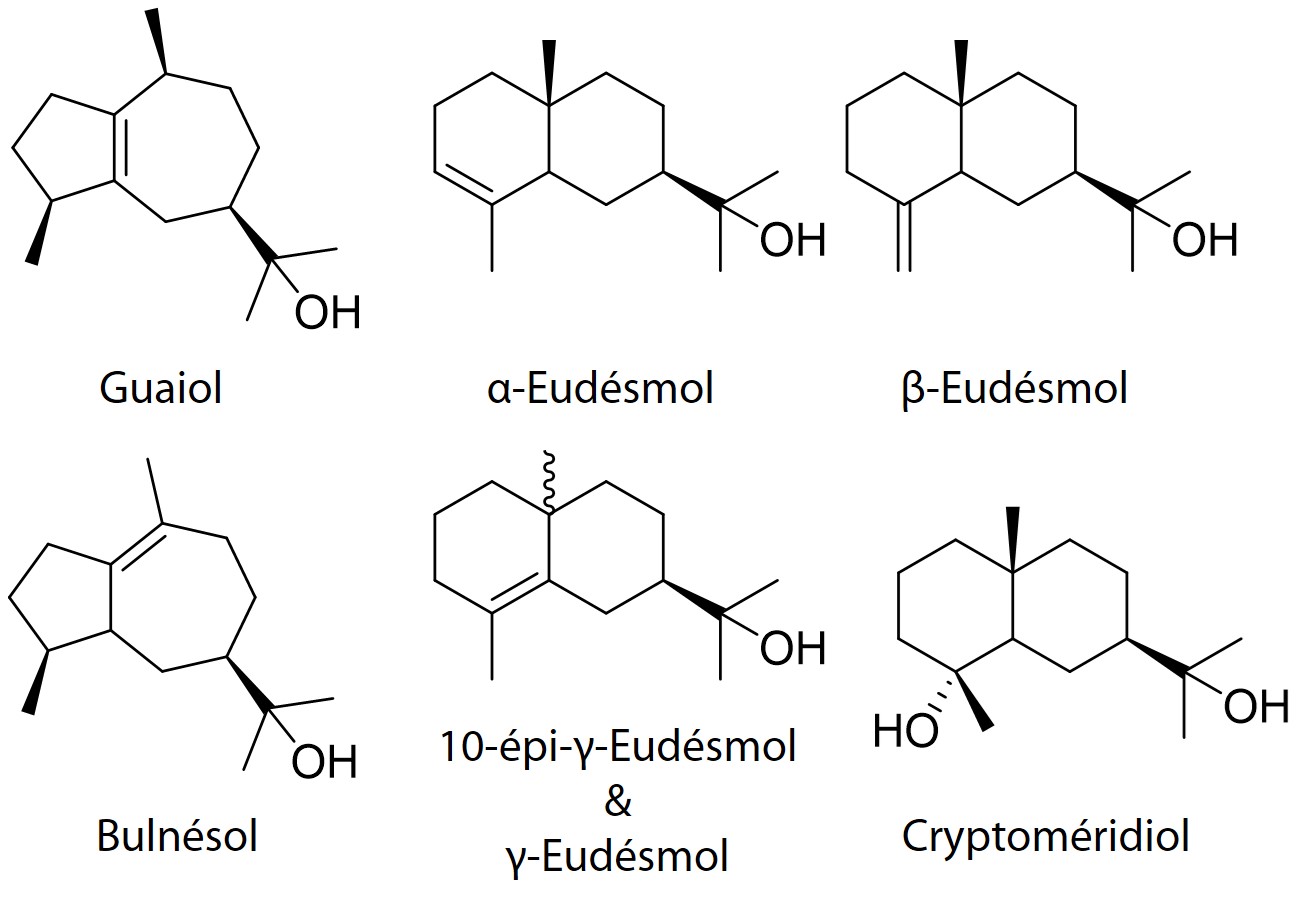
Figure 8. Composés corrélés dans une grappe de sesquiterpénols observés dans le cannabis. Aucun d’entre eux ne domine clairement les autres.
Le mot de la fin
Les proportions entre les terpènes peuvent constituer de bons outils pour décrire des variétés. Notre service d’analyse de terpènes complets est fourni avec une brève conclusion qui met en lumière les principales tendances relatives aux groupes discutés ci-haut, et nous continuons notre réflexion quant aux manières de repérer les tendances chémotypiques des terpènes du cannabis afin de mieux transmettre cette information à nos clients dans le futur.
Références
[1] Polatoglu, K. “Chemotypes”– A Fact That Should Not Be Ignored in Natural Product Studies. Nat. Prod. J. 2013, 3 (1), 10–14. https://doi.org/10.2174/2210315511303010004.
[2] de Meijer, E. The Chemical Phenotypes (Chemotypes) of Cannabis. In The Handbook of Cannabis; Pertwee, R. G., Ed.; Oxford University Press: Oxford, 2014; pp 89–110.
[3] Venditti, A. What Is and What Should Never Be: Artifacts, Improbable Phytochemicals, Contaminants and Natural Products. Nat. Prod. Res. 2020, 34 (7), 1014–1031. https://doi.org/10.1080/14786419.2018.1543674.
[4] Huang, A.-C.; Burrett, S.; Sefton, M. A.; Taylor, D. K. Production of the Pepper Aroma Compound, (−)-Rotundone, by Aerial Oxidation of α-Guaiene. J. Agric. Food Chem. 2014, 62 (44), 10809–10815. https://doi.org/10.1021/jf504693e.

